VIII抗HIV薬の作用機序と薬物動態
4.抗HIV薬の血中薬物濃度測定(TDM)
近年、第一選択薬として使用される抗HIV薬は、いくつかの組み合わせに集約される傾向にあるものの、抗HIV療法と日和見感染症治療を同時に施行する場合や、サルベージ治療に用いられる抗HIV薬の組み合わせは多様である。抗HIV薬の中でもNNRTIとPIはその薬物動態が相反しており、相互作用の強さは薬剤の組み合わせだけでなく、個体間によってもその動態が大きく変動する可能性がある。血中濃度測定の第一番目の意義は、治療効果の確認である。服薬アドヒアランスが十分であるにも関わらず血中HIV RNA量の再上昇があった場合、服薬開始後に血中HIV RNA量の十分な低下や低下速度に問題がある場合等があげられる。副作用等の有害事象が出現した場合も血中薬物濃度測定の対象となる。
抗HIV療法では多剤併用療法が行われることに加え、他の薬剤を併用する機会も数多く見られることから、治療効果はもちろんのこと、安全性の面からも、個々の薬物動態を十分に把握し、相互作用を理解しておくことが重要である。治療の失敗が許されないARTの特性を考えあわせると、治療は慎重に行われるべきであり、治療をより確実なものとするためにも、血中濃度測定を治療の選択肢として考慮すべき場合がある。
(1)血中濃度測定方法
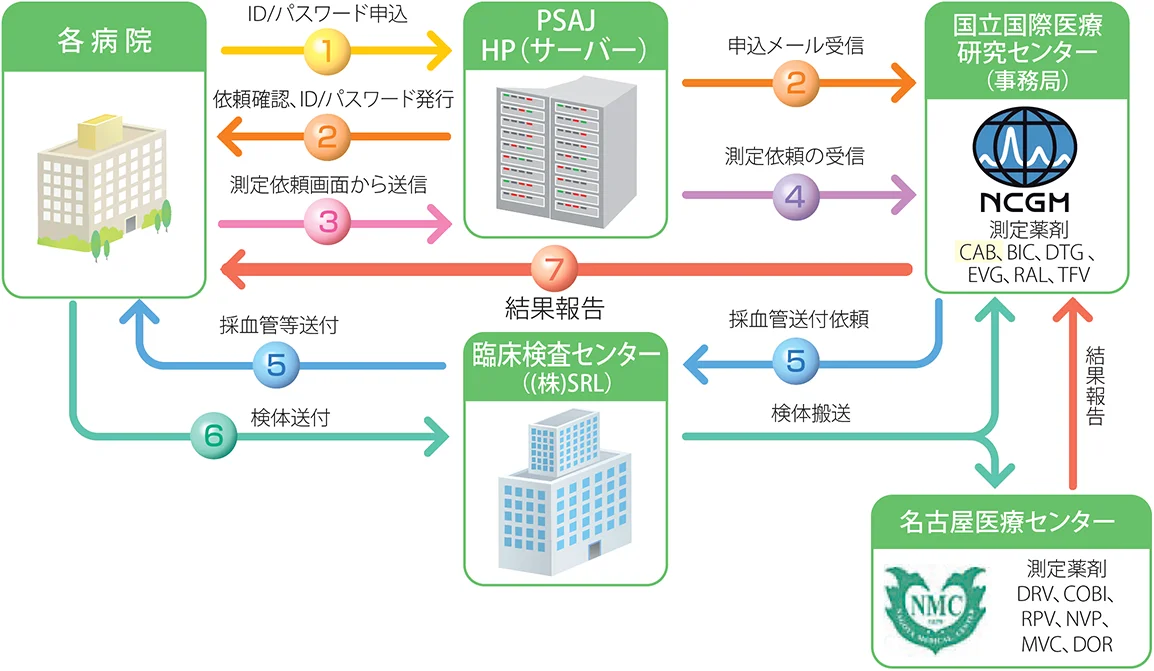
抗HIV薬の血中濃度測定については、日本医療研究開発機構エイズ対策実用化研究事業「抗HIV薬が薬剤耐性に与える影響についての研究(https://www.psaj.com/)」では研究班を経由して費用の負担なしで測定を依頼することができる。ホームページにアクセスし、ID・パスワードを取得後、必要事項と測定希望薬剤を入力する(図VIII-3)。
臨床現場において、抗HIV薬の血中濃度測定を検討する際の参考資料には、抗HIV薬血中濃度測定マニュアル(第3版)15)がある(PSAJホームページ)。
図VIII-3 依頼から検査結果報告までの流れ
(2)血中濃度測定が可能な抗HIV薬
2024年3月現在、NRTIのTFV、PIのDRV、ブースター剤のcobi、NNRTIのNVP、RPV、DOR、INSTIのRAL、EVG、DTG、BIC、CAB、CCR5阻害剤のMVCの血中薬物濃度測定が可能である。
(3)核酸系逆転写酵素阻害剤(NRTI)
NRTIの治療効果は活性型の細胞内濃度と相関する事が明らかであるが、治療効果と血中濃度との関連については、未だ明らかではない。NRTIは細胞内に入ってリン酸化された後に効果を発揮する一種のプロドラッグである。細胞側のリン酸化酵素によって三リン酸化体に変換され抗ウイルス効果を示すため、細胞内リン酸化酵素活性によってその効果が左右されることになる。細胞内における三リン酸化体の細胞内濃度について臨床的に応用する試みは行われていない。TDFおよびTAFは腸管から吸収後、TDFは殆どが、TAFはその一部がテノホビル(TFV)として血漿中に存在する。TFVは腎臓の尿細管において細胞障害を引き起こすことがあり、尿細管の機能障害を来している場合、尿細管の機能が正常な場合と比較して、TFV濃度が高値を示すことが示唆されている16)。
(4)非核酸系逆転写酵素阻害剤(NNRTI)
CAB+RPV注射剤において、第III相試験であるATLAS試験、FLAIR試験、ATLAS-2M試験を併合したCAB+RPVの投与歴のないHIV感染症患者の事後解析におけるリスク増加に関連した共変量は、プロウイルスのRPV耐性関連変異(RAM)、HIV-1サブタイプA6/A1(インテグラーゼ L74I多型と関連)、BMI≧30kg/m2以上(CABトラフ濃度と関連)及び注射初回投与4週後のRPVトラフ濃度の低下が挙げられている。このうち、ベースラインで認識しうる因子(RPV RAM、HIV-1 サブタイプ A6/A1 又は BMI≧30kg/m2)の2つ以上の組み合わせは、ウイルス学的治療失敗(CVF)リスクの増加との関連が報告されている17)。
初期CABおよびRPVのトラフ濃度を追加因子として含めた解析モデルでは、CVFのリスク上昇と関連し、CVFの予測はわずかに改善した。PK濃度を追加因子として考慮することは、リスクの減少につながる可能性がある18)。日常の臨床でのTDMの有用性は高くないが、患者背景を考慮してTDMを活用することが望まれる。
(5)プロテアーゼ阻害剤(PI)
現在の抗HIV療法では、rtvおよびcobiのCYP3A4およびP-gpに対する強力な阻害作用を積極的に利用し、併用するPIの血中濃度を高め、しかも長く持続させるためのブースターとして、少量のrtv(100mg程度)もしくはcobi(150mg)を併用する方法が用いられている。ブースターを用いることで、併用するPIの治療効果を高め、血中濃度を長く維持できるので、投与量や服用回数を減らすことが可能となる。
あらかじめrtvが配合されている薬剤にカレトラ®(LPV/rtv)、cobiが配合されている薬剤にプレジコビックス®(PCX)、シムツーザ®(SMT)がある。PIの血中濃度と薬剤耐性との関連については、血中濃度と抗ウイルス効果によって規定されるIQ(Inhibitory Quotient = Ctrough / IC50)値が大きいほど抗ウイルス効果は強く、長期に渡って効果が持続するとされている。しかし、血中濃度が高いと副作用の問題も発生するため、すべてのPIの血中濃度を高く保つことは不可能である。LPVはrtvと併用することによって血中濃度を比較的高く保っても副作用が発現しにくいとされ、IQ値を一定のレベル以上で保つことが出来る薬剤である。
(6)インテグラーゼ阻害剤(INSTI)
RALの臨床試験(フェーズII、III)において、RALの血中濃度が治療効果に及ぼす影響は少なかったとされているが19)、in vitroにおいて濃度相関を示したとする報告もある20)。また、DTGについては実臨床において、血中濃度高値と精神神経系の有害事象の関連が示唆されている21)。
(7)侵入阻害剤(CCR5阻害剤)
MVCをCYP3A阻害剤又はCYP3A誘導剤と併用する場合は、用量調整が必要とされている。例えばPI、イトラコナゾール、クラリスロマイシン等の強力なCYP3A阻害剤と併用する場合、MVCの用量は150mgを1日2回へ減量する。NVPやNRTIと併用する場合MVCの用量は300mgを1日2回とする。RFP等の強力なCYP3A誘導剤と併用する場合MVCの用量は600mgを1日2回へ増量することとされている。MVCは併用薬の影響を大きく受ける薬剤であり、日本人での薬物動態は不明である。本剤を投与する場合は血中濃度をモニタリングすることが望ましい。
(8)目標(参考)とする血中濃度
HIV-1野生株に対する目標トラフ濃度を表VIII-3-1に、DRV(1200mg 分2)、RALについては、過去の臨床試験で測定されたトラフ濃度の中央値を表VIII-3-2に示す22, 23)。また、RPV(経口)、DOR、DRV(800mg 分1)、RAL、EVG、DTG(50mg 分1)、BICおよびCAB+RPV(注射)については、報告されている日本人HIV-1感染者を対象としたトラフ濃度の中央値24-31)を表VIII-3-3、VIII-3-4に示す。
表VIII-3-1 HIV-1野生株に対する目標トラフ濃度
| 薬剤名 | 濃度 |
|---|---|
| LPV | 1,000 |
| RTV | 2,100 |
| NVP | 3,000 |
| MVC | >50 |
表VIII-3-2 過去の臨床試験で測定されたトラフ濃度の中央値(範囲)
| 薬剤名 | 濃度 |
|---|---|
| DRV |
3,539 |
| RAL | 72 |
表VIII-3-3 日本人を対象とした検討で報告されているトラフ濃度の中央値
| 薬剤名 | 症例数 | 中央値 |
|---|---|---|
| RPV(経口) | 33 | 66 |
| DOR | 11 | 626 |
| DRV |
70 | 1,587 |
| RAL | 114 | 170 |
| EVG | 50 | 410 |
| DTG |
107 | 1,060 |
| BIC | 44 | 3,750 |
表VIII-3-4 日本人を対象とした検討で報告されているトラフ濃度の中央値
| 薬剤名・投与方法 | 症例数 | 中央値 |
|---|---|---|
| CAB+RPV 12週 |
4 | CAB:644(392-2,162) RPV:46(31-84) |
| CAB+RPV 44週 |
5 | CAB:1,504(796-2,365) RPV:51(36-103) |