IX抗HIV薬の副作用
要約
- HIV感染症に対する治療として多剤併用療法が行われるようになり、HIV感染症の予後は劇的に改善した。また、近年副作用の少ない薬剤の開発承認がすすめられてきている。しかし、一方では抗HIV薬の長期内服に伴う副作用が後になって分かってくることもある。さらに、薬剤変更後に副作用があったことに初めて気が付く場合もあるため、治療開始およびその後の経過においては慎重な観察が必要である。
- 抗HIV療法によって予後が改善してきた一方で、様々な長期合併症が新たな問題となってきた。心血管疾患、慢性腎臓病、骨関連疾患、精神・神経疾患、糖・脂質代謝障害、体重増加などは、抗HIV薬による副作用の影響を受ける可能性があり、必要に応じて薬剤変更なども考慮しなければならない。
- 抗HIV薬を初めて使用する場合には各薬剤の添付文書を必ず確認していただきたい。独立行政法人医薬品医療機器総合機構(PMDA;Pharmaceuticals and Medical Devices Agency)のホームページ(https://www.pmda.go.jp/PmdaSearch/iyakuSearch/)にアクセスすることで、その時点で最新の添付文書を見ることができる。選択した各々の薬剤の副作用頻度については、第V章 表V-6を参照されたい。
1.代謝異常と動脈硬化性疾患
抗HIV薬の脂質代謝への影響は、薬剤によって異なる。非核酸系逆転写酵素阻害剤(NNRTI)の中でDORは、初回治療におけるEFV(販売中止)との比較、あるいはEFVからDORへの変更においてEFVよりも脂質に関する有害事象が少なかった。同様のことはプロテアーゼ阻害剤(PI)であるDRV+rtvとDORの比較試験でも報告されている1)。NNRTIであるRPVも脂質異常に関して、EFVやrtvブーストのPIと比較して良好な安全性プロファイルを持っている2)。PIは一般的に脂質代謝異常を起こしやすいが、DRV+rtvは脂質代謝への影響が少ない3, 4)。また、DRV+rtvからDRV/cobiへの変更に伴い、TGおよびTC、LDL-Cが低下したとの報告がある5)。インテグラーゼ阻害剤(INSTI)はPIに比べ、脂質代謝異常を起こしにくいことが知られている6)。INSTIの中ではEVG/cobiでTG増加、LDL増加、HDL増加が認められる。核酸系逆転写酵素阻害剤(NRTI)のなかでTAFはHIV陽性者において総コレステロール、LDLおよびHDLコレステロール、およびTG増加との優位な関連が示された。メタ回帰分析では、若年年齢、男性、および低BMIがコレステロール値増加の危険因子であった7)。またTDFは、ABC、TAFと比べ、むしろ脂質を低下させることが報告されている8-10)。
ART施行中の患者では、インスリン抵抗性の増大に伴い糖代謝異常の頻度が増加することも知られている8)。これは、各種薬剤によるミトコンドリア機能障害やインスリンシグナル伝達の異常8)、脂肪細胞のPPARγ発現量がNRTIにより低下すること、glucose transporter 4を介した糖の膜輸送がPIにより障害されることなどが関与していると考えられている11)。最近、INSTI使用(初回治療および治療変更)34,398例のデータベースの解析においてINSTIの使用ではINSTI以外と比較して糖尿病および高血糖の発生が多く、INSTIの中ではDTGで最も顕著でRALでは関連が認められなかったことが報告されている12)。特にINSTIへ変更後の早期の体重増加がインスリン抵抗性に関与していたと報告されている13)。
また、TAFベースレジメンからDTG/3TCの2剤療法への変更では144週の時点で脂質の改善が認められたがHOMA-IRによるインスリン抵抗性は両群で差を認めなかった14)。
ARTをほぼ生涯にわたって継続しなくてはならない現状を考えると、これらの代謝異常症の合併は虚血性心疾患や脳血管障害などの動脈硬化を基盤とする生活習慣病のリスクを増加させる。D:A:D(Data collection on Adverse events of anti-HIV Drugs)調査グループの報告では、ARTの施行期間が長いほど虚血性心疾患と脳血管障害の頻度が増加し、1年のARTへの曝露で年間発生率が26%増加することを示している15, 16)(図IX-1)。また、NNRTIに比べPIにおいて、心筋梗塞の発生率が高いことも示している17, 18)(図IX-2)。さらに、NRTIについては、ABCと心筋梗塞リスクの関連について相反する結果が出ている19-23)。D:A:D調査グループは、より長期にわたり大規模コホートの解析を継続し、ART全体によるリスクとともにABC使用による心筋梗塞の関連性を再び指摘した23)。CVDとINSTIの関連では、初回治療例にINSTIおよびINSTI以外を使用し各々CVDの発生頻度を比較した試験において、多変量解析では両群の発生頻度に差を認めなかった24)。HIV感染者においては、HIVそのものが脂質代謝や血管内皮機能に影響を与えているとする報告もあり25, 26)、心血管系に影響を及ぼす因子は多岐に及ぶため、さらなる大規模調査による検討が必要である。HIV感染症における長期治療経過において背景に存在する糖・脂質代謝異常、高血圧、高尿酸血症、肥満、喫煙などの危険因子をコントロールしていくことも重要である。
ART開始にあたっては代謝異常のリスクファクターを評価し、禁煙や肥満の是正などの適切な生活指導を行うとともに、リスクがある場合は代謝への影響が少ない薬剤を選択する。また、スタチン系またはフィブラート系の薬剤の投与も検討する。「REPRIEVE試験」では、CVDリスクが低~中等度の40~75歳のART中のHIV感染者において、ピタバスタチンはプラセボと比較し、追跡期間中央値5.1年で主要有害心血管イベント(CVDによる死亡、心筋梗塞、不安定狭心症による入院、脳卒中、一過性脳虚血発作、末梢動脈虚血、血行再建術、原因不明の死亡)のリスクを低下することが示された27)。また炎症性メディエーターの減少、非石灰化プラークの縮小も認められた28)。スタチン系薬剤は、CYP3A4によって代謝されるので、PIやcobiを含むレジメンとの併用には注意が必要であり、一部のスタチン系薬剤は、これらの薬剤と併用禁忌となっているので実際に使用する際は添付文書で確認する。NNRTIとの併用時には、スタチン系薬剤の増量が必要な場合がある。一方、フィブラート系薬剤は、CYP3A4ではなくCYP4Aによって代謝されるので、抗HIV薬との相互作用は問題とならない。なお、高脂血症を含むHIV感染症に合併する疾患のプライマリケアについては、米国におけるIDSAのガイドライン29)、欧州におけるEACSガイドライン30)が出されており、その対応について理解する上での参考となる。
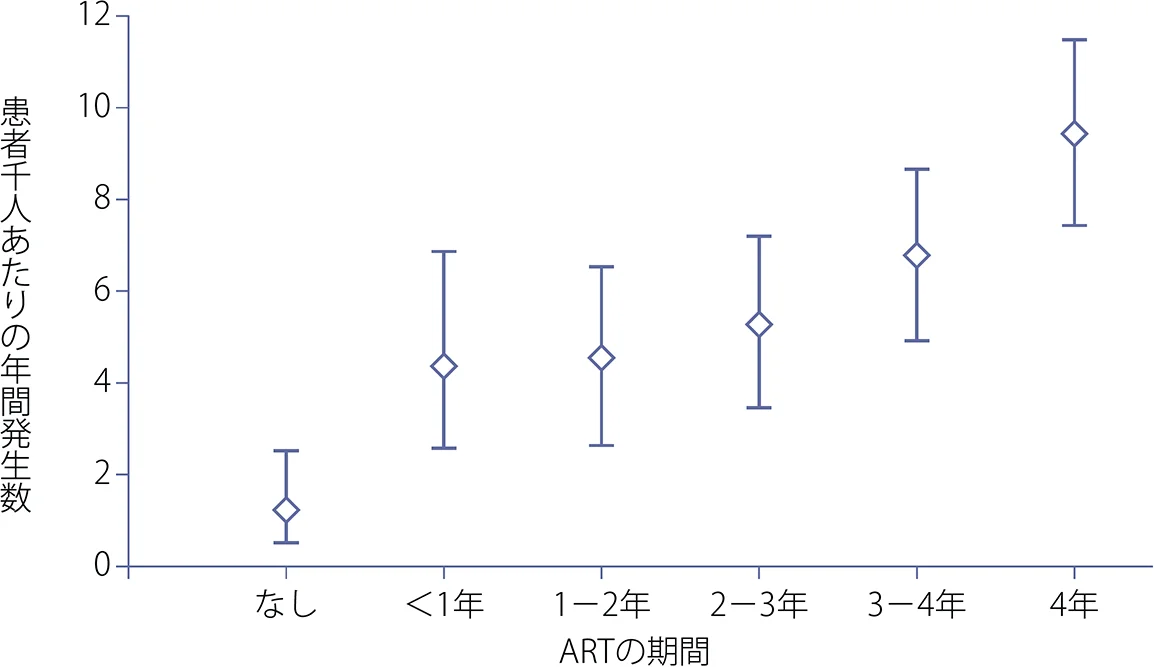
図IX-1 ARTの期間と心・脳血管障害の発生頻度
図IX-2 NNRTI及びPI投与期間と心筋梗塞の発生頻度
A
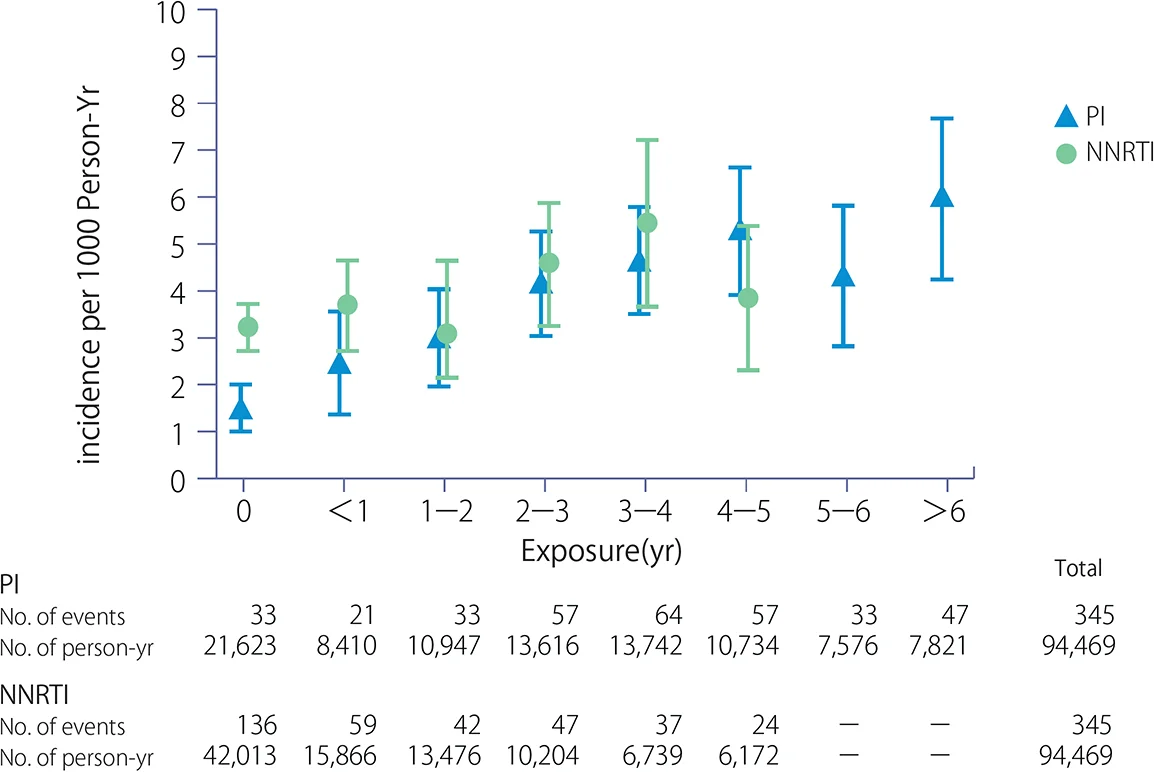
B