VII治療失敗時の薬剤変更
3.薬剤耐性検査(遺伝子型)の解釈と治療薬の変更
薬剤耐性検査には、ウイルス遺伝子の塩基配列を調べて変異アミノ酸を見つける遺伝子型解析(genotypic assay)と抗ウイルス薬の存在下でウイルスの増殖をみる表現型解析(phenotypic assay)がある。現在日本で保険収載されている耐性検査(HIV-1ジェノタイプ薬剤耐性検査)は遺伝子型解析であり、本ガイドラインでは遺伝子型の耐性検査についてのみ言及する。
(1)薬剤耐性検査(遺伝子型)の基礎知識
抗HIV薬を内服している(はずの)患者において血中HIV RNA量のコントロールが不良な場合は、薬剤耐性HIVの出現の可能性を念頭におき薬剤耐性検査を行う必要がある。耐性検査により治療失敗の原因を明らかにすることが出来るし、ARTレジメンを変更する際の重要な情報となる。薬剤耐性検査を行う際には、以下の2点を念頭におく必要がある。
- 耐性検査は原則として薬剤服用中に実施しなくてはならない
- 耐性HIVが患者体内のHIVの30%程度以上を占めないと検出されない
耐性HIVを有する患者体内には野生型HIVも共存している。ウイルスの増殖スピードの点から見ると、薬剤の作用部分に変異が生じている耐性株の増殖スピードは、野生型のそれより劣ることが多いため、薬剤中断後には野生型HIVが耐性HIVを凌駕して増殖する。そのため、治療中断後は耐性HIVの頻度は次第に低下していくことになる。耐性検査(遺伝子型)では野生株も耐性株もまとめて遺伝子配列を決定するため、患者体内のHIVのうち耐性HIV株が約30%以上にならなければ薬剤耐性変異株を検出することができない。そのため、治療中止後、つまり抗HIV薬の血中濃度が低下し野生型の増殖が回復した状態で耐性検査を行い薬剤耐性変異が検出されなくとも、本当に耐性を生じていなかったのか、耐性HIVの比率が減少したため検出されなかったのかは判断できない。逆に、血中HIV RNA量がコントロールできていない症例の治療中の検体で薬剤耐性変異が検出されない場合は、その患者が薬剤を内服していなかったことが強く疑われる。
(2)薬剤耐性検査(遺伝子型)の結果に基づく抗HIV療法の変更
治療失敗時に、薬剤耐性検査の結果を参考にして薬剤変更した群と過去の治療歴の情報のみを参考にして薬剤変更した群との比較では、前者で有意に良好な成績が得られており16)(図VII-2)、治療変更を考える際に耐性検査は必須である(AI)。
耐性検査(遺伝子型)では、HIV逆転写酵素、プロテアーゼ、インテグラーゼ、およびカプシドのどのアミノ酸部位に変異が起きているかという結果が表示される(図VII-3-1)。また、これまでの耐性HIV株の薬剤感受性のデータの蓄積から、これらのアミノ酸変異と各薬剤の耐性の程度の間には図VII-3-2に示すような関係が明らかになっており17)、この情報から耐性検査結果を解釈することになる。以下に耐性変異とその解釈の例をあげる。
図VII-2 Salvage治療の効果と耐性検査
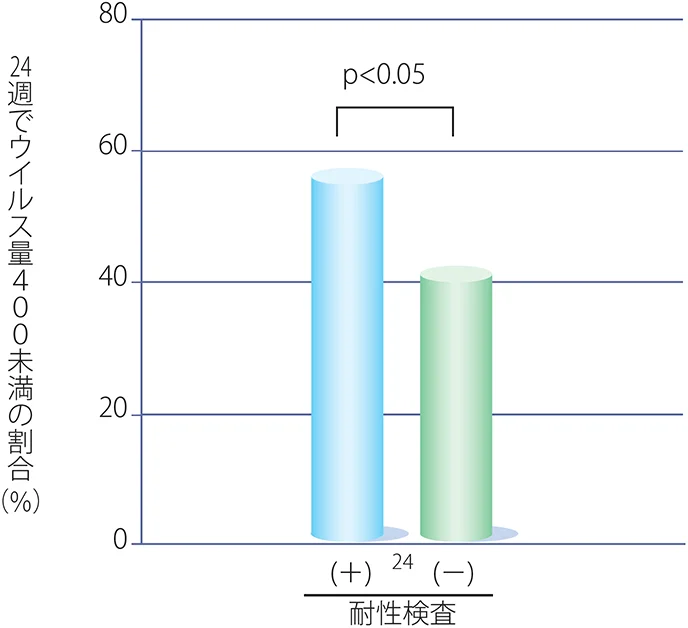
Tural et al. AIDS. 16: 209, 2002 より。
図VII-3-1 薬剤耐性変異

- <例1>逆転写酵素の41番のアミノ酸がL(ロイシン)に変異
- → AZTに軽度の耐性、ABC、3TC、TDF、FTCは影響を受けない
- <例2>逆転写酵素の184番のアミノ酸がV(バリン)に変異
- → 3TCとFTCに対しては高度の耐性となるが、AZTとTDFに対してはむしろ感受性が増強する
- <例3>逆転写酵素の103番のアミノ酸がN(アスパラギン)に変異
- → EFV(販売中止)に対して高度耐性、RPV、DORは影響を受けない
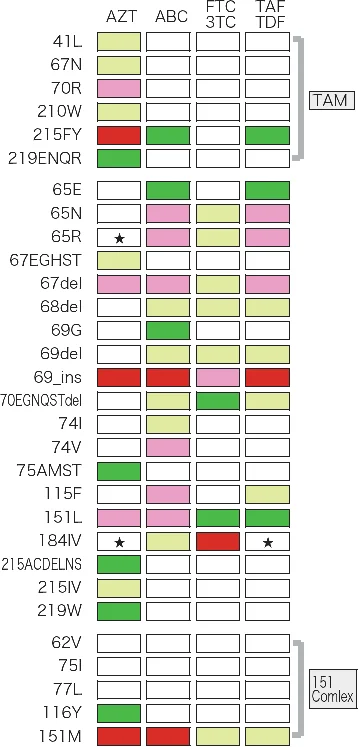
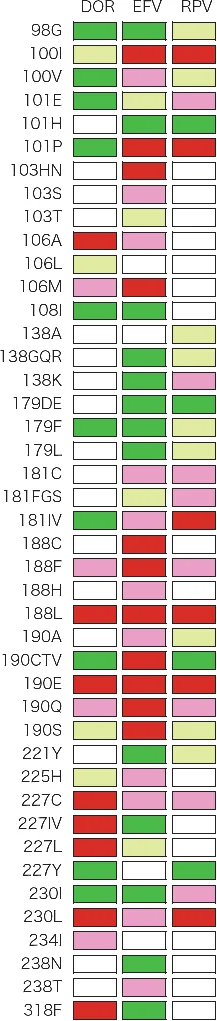
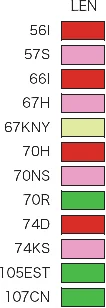
図VII-3-2 それぞれの薬剤耐性変異の感受性への影響
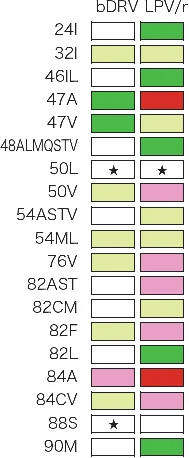
cobiでブーストされたDRV

高度耐性
中等度耐性
軽度耐性
耐性に寄与
耐性なし
★ 感受性増加
パネル左端に示すアミノ酸変異が生じた場合に、パネル上端の抗HIV薬に対してどのような耐性が生じるかを色別に表したもの。
Stanford大学のHIV Drug resistance databaseをもとに作成。
遺伝子型耐性検査のやっかいな点は、アミノ酸変異が蓄積するにつれて個々の変異の耐性を表示した図VII-3-2からだけでは各薬剤の耐性の程度を読み取ることが次第に難しくなることである。特に、NRTI耐性に関連した変異の中には、ある薬剤への耐性変異が他の薬剤に対する感受性を増加させるものがあり、その解釈をさらに複雑にさせている。簡便な方法として、種々のアミノ酸変異をもつ臨床分離HIV株の表現型耐性検査の結果がデータベース上で公開されており、それを参照することで遺伝子型耐性検査の結果を表現型(IC50)に置き換えることが出来る(IC50とは、HIVの増殖を50%抑制するのに必要な抗HIV薬の濃度である)。表VII-2に、変異が蓄積すると耐性の程度がどのように変化するかについての一例を示す。表中の数字は、野生株のIC50を1とした場合の患者由来HIV株のIC50の相対比(IC50比)である。したがって1未満であれば感受性が増強していることを示し、1を超えてIC50比が増加するほど薬剤耐性が増すことになる。ただし、NRTIの場合薬物血中濃度よりも細胞内濃度の方が抗ウイルス活性に重要であると考えられ、表現型検査で得られるIC50比が必ずしもin vivoの効果を反映しない可能性がある。また、PIの場合は少量rtvやcobicistatをCYP3A阻害剤として用い高いトラフ値を得ることができるため(いわゆるboosted PI)、IC50比が上昇しても臨床的に抗ウイルス効果が持続する。この傾向はLPV/rtvで最も顕著で、LPV/rtvのトラフ値はLPV単剤のIC50の70倍以上にも達する18)。そのため、LPV耐性変異の中でIC50比が70倍までの変異を持つHIVにはLPV/rtvの抗ウイルス効果が期待できることになる。一方、NNRTIのうちNVP(販売中止予定)やEFV(販売中止)に対する耐性変異の多くは1つのアミノ酸置換で高度耐性となることが多く、その解釈は比較的容易である。
表VII-2 変異の蓄積による表現型耐性検査結果(IC50比)の変化の例
| AZT | TDF | ABC | 3TC | |
|---|---|---|---|---|
| 184V | 0.5 | 0.5 | 3.1 | 200 |
| 65R | 0.5 | 1.8 | 2.4 | 8.7 |
| 65R, 184V | 0.4 | 1.2 | 8.4 | 200 |
| 41L, 215Y | 12 | 1.3 | 2.0 | 2.0 |
| 41L, 215Y, 184V | 6.0 | 1.1 | 5.1 | 200 |
| 41L, 215Y, 210W | 164 | 3.1 | 3.1 | 2.8 |
| 41L, 215Y, 210W, 184V | 18 | 1.6 | 6.5 | 200 |
獲得した変異のパターンから薬剤耐性のレベルを評価する方法に関しては、いくつかの研究グループが独自のアルゴリズムを公開している。
- スタンフォード薬剤耐性データベース(https://hivdb.stanford.edu/)
- The Agence Nationale de Recherche sur le SIDA(ANRS)薬剤耐性評価
(https://hivfrenchresistance.org/) - Rega Institute in Leuven, Belgium の研究グループが開発したものなどである。
これらの中で、比較的簡便で広く用いられているスタンフォード薬剤耐性データベースの使い方について述べる。
- 手順1
- https://hivdb.stanford.edu/にアクセスする。トップページ右上の「HIVdb Program」をクリックすると、薬剤耐性解析のページに切り替わる。
- 手順2
- アミノ酸配列のプルダウンメニューを操作して、どのアミノ酸がどのように変化したかを入力する。
- 手順3
- 画面右下にある「Analyze」をクリックすると、どの薬剤に耐性でどの薬剤に感受性があるかを表示する結果画面が現れる。
(薬剤耐性検査の詳細については、日本医療研究開発機構 エイズ対策実用化研究事業「国内流行HIV及びその薬剤耐性株の長期的動向把握に関する研究」班による「HIV薬剤耐性検査ガイドラインver.10」19)も参照していただくとよい。https://www.hiv-resistance.jp/resistance04.htmからダウンロード可能)
以上のことを参考に、耐性検査の結果から効果が期待できる複数の抗HIV薬を選択しSalvage治療を行うことになる。抗ウイルス効果を優先させた選択になるので、Salvage治療で選択されるARTレジメンは、同時代における推奨初回レジメンに比べ飲みにくい組み合わせにならざるを得ない。耐性HIVが出現する背景には服薬率の低下が密接に関連しているので、高い服薬率が得られる確信がなければ安易にSalvage治療に変更すべきでない。ただし、新しい世代の薬剤は、有害事象や錠剤数・大きさの観点で服用がより容易となっているものが多いことから、適切な組み合わせを選択することにより服薬率の向上につなげられる可能性もある。その判断にはある程度の経験と知識が必要であり、自信を持った選択が出来ない場合は経験豊富な医師と相談しつつ決定するのがよい。